Lavoiser miktarÄą belli olan kalay (Sn) parcĖ§asÄąnÄą icĖ§inde bir miktar hava bulunan bir fanusa koyarak tartmÄąsĖ§. Daha sonra fanusu icĖ§indekilerle birlikte ÄąsÄątmÄąsĖ§ ,ÄąsÄąnan kalayÄąn beyaz bir toz haline ( Sn O )doĖnuĖsĖ§tuĖgĖuĖnuĖ goĖzlemlemisĖ§tir. OlusĖ§an beyaz tozu ve fanusu tekrar tarttÄągĖÄąnda basĖ§langÄącĖ§ta belirledigĖi kuĖtle ile esĖ§it oldugĖunu goĖzlemlemisĖ§tir.
Benzer deneylerle aynÄą sonuca ulasĖ§mÄąsĖ§tÄąr. OlusĖ§an beyaz tozu (Kalay oksit ) benzer yolla ÄąsÄąttÄągĖÄąnda ise basĖ§langÄącĖ§ta fanusa koydugĖu KalayÄąn kuĖtlesin esĖ§it kuĖtlede kalay elde ettigĖini goĖzluĖyor ve kendisini unutulmaz yapan sĖ§u sonuca varÄąyor.â
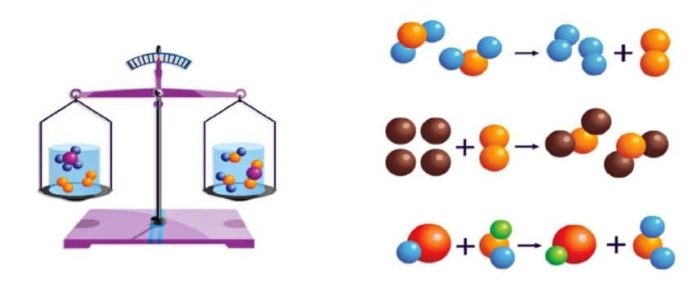
Madde yoktan var edilemedigĖi gibi, vardan da yok edilemez. Sadece birinden oĖtekine doĖnuĖsĖ§ebilirâ
Bu ifadesi "KuĖtlenin Korunumu YasasÄą" diye bilinir
Bu guĖnkuĖ ifadesi ile;
Kimyasal olaylarda, tepkimeye giren maddelerin kuĖtleleri toplamÄą, tepkime sonunda olusĖ§an maddelerin kuĖtleleri toplamÄąna esĖ§ittir. Bu olaya KUĖTLENIĖN KORUNUMU KANUNU denir.
KuĖtlenin Korunumu Kanunu
1. Erime,donma,buharlasĖ§ma,yogĖunlasĖ§ma gibi hal degĖisĖ§imleri ile cĖ§oĖzuĖnme gibi fiziksel olaylarda da korunur.
2. Kimyasal olaylara giren maddelerin kuĖtleleri toplamÄą, elde edilen uĖruĖnlerin kuĖtleleri toplamÄąna esĖ§ittir.
OĖRNEK;
Bir parcĖ§a magnezyumun tuĖmuĖ 98 gr suĖlfuĖrik asit ile tepkimeye giriyor. OlusĖ§an magnezyum suĖlfatÄąn kuĖtlesi 120 gr ve acĖ§ÄągĖa cĖ§Äąkan hidrojenin kuĖtlesi ise 2 gr oldugĖuna goĖre kullanÄąlan magnezyum kacĖ§ gramdÄąr.
Magnezyumun kuĖtlesi + SuĖlfuĖrik Asidin kuĖtlesi = Magnezyumun suĖlfatÄąn kuĖtlesi + Hidrojenin kuĖtlesi
? + 98 = 120gr + 2gr
KuĖtlenin korunumu kanununa goĖre;
Magnezyumun kuĖtlesi + 98 = 120 + 2
Magnezyumun kuĖtlesi = 24 gr dÄąr.
Benzer deneylerle aynÄą sonuca ulasĖ§mÄąsĖ§tÄąr. OlusĖ§an beyaz tozu (Kalay oksit ) benzer yolla ÄąsÄąttÄągĖÄąnda ise basĖ§langÄącĖ§ta fanusa koydugĖu KalayÄąn kuĖtlesin esĖ§it kuĖtlede kalay elde ettigĖini goĖzluĖyor ve kendisini unutulmaz yapan sĖ§u sonuca varÄąyor.â
Madde yoktan var edilemedigĖi gibi, vardan da yok edilemez. Sadece birinden oĖtekine doĖnuĖsĖ§ebilirâ
Bu ifadesi "KuĖtlenin Korunumu YasasÄą" diye bilinir
Bu guĖnkuĖ ifadesi ile;
Kimyasal olaylarda, tepkimeye giren maddelerin kuĖtleleri toplamÄą, tepkime sonunda olusĖ§an maddelerin kuĖtleleri toplamÄąna esĖ§ittir. Bu olaya KUĖTLENIĖN KORUNUMU KANUNU denir.
KuĖtlenin Korunumu Kanunu
1. Erime,donma,buharlasĖ§ma,yogĖunlasĖ§ma gibi hal degĖisĖ§imleri ile cĖ§oĖzuĖnme gibi fiziksel olaylarda da korunur.
2. Kimyasal olaylara giren maddelerin kuĖtleleri toplamÄą, elde edilen uĖruĖnlerin kuĖtleleri toplamÄąna esĖ§ittir.
OĖRNEK;
Bir parcĖ§a magnezyumun tuĖmuĖ 98 gr suĖlfuĖrik asit ile tepkimeye giriyor. OlusĖ§an magnezyum suĖlfatÄąn kuĖtlesi 120 gr ve acĖ§ÄągĖa cĖ§Äąkan hidrojenin kuĖtlesi ise 2 gr oldugĖuna goĖre kullanÄąlan magnezyum kacĖ§ gramdÄąr.
Magnezyumun kuĖtlesi + SuĖlfuĖrik Asidin kuĖtlesi = Magnezyumun suĖlfatÄąn kuĖtlesi + Hidrojenin kuĖtlesi
? + 98 = 120gr + 2gr
KuĖtlenin korunumu kanununa goĖre;
Magnezyumun kuĖtlesi + 98 = 120 + 2
Magnezyumun kuĖtlesi = 24 gr dÄąr.
OĖRNEK;
40 ml KuĖkuĖrt di oksit gazÄąnÄąn 32 gr oksijenle tepkimesinden 160 gr KuĖkuĖrt tri oksit olusĖ§tugĖuna goĖre KuĖkuĖrt di oksitin aynÄą kosĖ§ullarda oĖz kuĖtlesi nedir?
KuĖkuĖrt di oksit gazÄą kuĖtlesi + oksijen gazÄą kuĖtlesi = ? + 32 gr
KuĖkuĖrt di oksit gazÄą kuĖtlesi + 32 = 160
KuĖkuĖrt di oksit gazÄą kuĖtlesi = 128 gr
KuĖkuĖrt di oksit gazÄą oĖz kuĖtlesi = m / V
KuĖkuĖrt di oksit gazÄą oĖz kuĖtlesi = 128 gr / 40mlt
KuĖkuĖrt di oksit gazÄą oĖz kuĖtlesi = 3.2 gr / mlt
OĖRNEK;
KuĖkuĖrt di oksit gazÄą kuĖtlesi + 32 = 160
KuĖkuĖrt di oksit gazÄą kuĖtlesi = 128 gr
KuĖkuĖrt di oksit gazÄą oĖz kuĖtlesi = m / V
KuĖkuĖrt di oksit gazÄą oĖz kuĖtlesi = 128 gr / 40mlt
KuĖkuĖrt di oksit gazÄą oĖz kuĖtlesi = 3.2 gr / mlt
OĖRNEK;
KuĖkuĖrt tri oksit gazÄą kuĖtlesi = 160 gr
Saf olmayan 8 gr magnezyum 14,6 gr hidroklorik asitle reaksiyondan 19 gr magnezyum kloruĖr ile 0,4 gr hidrojen gazÄą olusĖ§uyor. Magnezyumun yuĖzde kacĖ§Äą reaksiyona girmisĖ§tir?
Mgâmun kuĖtlesi + Hidroklorik Asidin kuĖtlesi = Mgâmun kloruĖruĖn kuĖtlesi + Hidrojen gazÄąnÄąn kuĖtlesi
? + 14,6 gr = 19 gr + 0,4 gr
KuĖtlenin korunumu kanununa goĖre;
Magnezyumun kuĖtlesi + 14,6 = 19 + 0,4
Magnezyumun kuĖtlesi = 4,8 grâdÄąr
8 gr Magnezyumdan kimyasal reaksiyona giren magnezyum kuĖtlesi 4,8 gr dÄąr
100 gr Magnezyumdan kacĖ§ gr magnezyum reaksiyona girer?
8 gr â 4,8 gr
100 â ?
? = (100 x 4,8) / 8
? = % 60 â reaksiyona girmisĖ§tir.
Mgâmun kuĖtlesi + Hidroklorik Asidin kuĖtlesi = Mgâmun kloruĖruĖn kuĖtlesi + Hidrojen gazÄąnÄąn kuĖtlesi
? + 14,6 gr = 19 gr + 0,4 gr
KuĖtlenin korunumu kanununa goĖre;
Magnezyumun kuĖtlesi + 14,6 = 19 + 0,4
Magnezyumun kuĖtlesi = 4,8 grâdÄąr
8 gr Magnezyumdan kimyasal reaksiyona giren magnezyum kuĖtlesi 4,8 gr dÄąr
100 gr Magnezyumdan kacĖ§ gr magnezyum reaksiyona girer?
8 gr â 4,8 gr
100 â ?
? = (100 x 4,8) / 8
? = % 60 â reaksiyona girmisĖ§tir.
2019-11-27 Admin Admin
Taglar: KÞtleninKorunumuKanunu
| Kimya Ders NotlarÄą - Ä°lginizi çekebilecek baÅlÄąklar |
|---|
|
BileÅiklerin OluÅmasÄą ve Ãzellikleri
GÞnÞmÞzde bilinen 117 element olmasÄąna raÄmen (92 tanesi doÄada bulunur) bu elementler farklÄą sayÄąda ve Åekilde birleÅerek ve etkileÅerek farklÄą kimyasal Ãķzelliklere sahip milyonlarca yani madde yani bileÅik oluÅtururlar. |
|
KatlÄą Oranlar Kanunu
âiki element aralarÄąnda birden fazla bileÅik oluÅturuyorsa, bunlardan birinin sabit miktarÄąyla birleÅen ikincisinin deÄiÅen miktarlarÄą arasÄąnda basit tam sayÄąlÄą bir oran bulunur.â Bu Åekilde âKatlÄą Oranlar Kanunuâ olarak bildiÄimiz y |
|
Organik Kimya Ders NotlarÄą
Organik Kimya Ders NotlarÄą Ãķzetleri; Kuantum Sayilari ve Periyodik Sistem. Periyodik Ãzellikler ve Elementler. Gazlar. ÃÃķzelti EtkileÅimleri ve DeriÅimleri. Kimyasal Tepkimelerde Enerji |



Sayfa YorumlarÄą